本章では, シミュレーション実験について述べる. 本セクションの前半では, 実験に用いた心筋細胞電気生理学モデルのKyoto
model, シミュレーションソフト『E-CELL
System』, モデリングの概要と分岐解析について説明する. 後半では, シミュレーション実験方法について具体的に述べる.
洞房結節の活動電位と各イオン電流モデル構造
イオン電流には内向きと外向き電流が存在する. 洞房結節における活動電位と各イオンチャネル電流の関係を, 外向き内向きに分けて図に示した. 縦軸の大きさは電流により異なる.
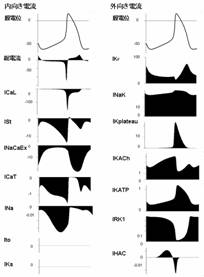
図 1 活動電位とイオン電流
1.1.1.
対象
シミュレーションにはKyoto model洞房結節細胞モデルを用いた.
a.
目的
Krノックアウト実験のコントロールを取る. 各チャネルに対するモデルの耐性を調べる.
b.
方法
コンダクタンスは通りやすさの指標を表すもので, チャネルの発現量に比例するものである. その値を調節することで各イオン電流量を設定した.各チャネルの透過係数にあたるパラメータを0%から200%まで50%刻みで活性量を変えた.シミュレーションは計算結果が完全に安定した後のデータを用いるために, 300秒行った. データの比較においては, 任意の0.79秒(約2周期分)のデータを用いた.
c.
パラメータ一覧
シミュレーション実験で用いた, 各イオンチャネルのパラメータは下記の通りである.
表 1 パラメータ一覧

1.1.3.
Kr抑制実験
a.
目的
自律的な活動電位の形成に必須であるKrチャネルの活性が心筋細胞の電気生理学的な現象に及ぼす影響を見る.
b.
方法
正常状態のモデルとKrの活性を変化させたモデルの膜電位を比較した. シミュレーションにおける初期値は, Kyoto modelで用いられている初期値を使用した. Kyoto model では, Krチャネルの式は, 式1のようにあらわされている.
Kr ionic current = (FF*AF + FS*AS) * IN * gKr * R * CF (式1)
FF: fast coefficient AF: fast active gate open probability FS: slow coefficient coefficient AS: slow active gate open probability IN: inactive gate open probability gKr: conductance R: permeability ratio CF: diffusion formula
Krチャネルのコンダクタンスに関する係数gKrは, Krチャネルの数に比例している. 活性イオンチャネル分子数の増減は, gKrの増減によって表現し, 各活性状態についてシミュレーションを行った. シミュレーションが安定状態に達した, シミュレーション開始後180秒から300秒の120秒間のデータを解析に用いた. 活性の影響を詳細に考察する為に, モデル中の定数以外の全変数の時系列を記録した.
2.1. 影響
各チャネルの活性と膜電位の相関をシミュレーションにより確認した. 膜電位への影響を比較するため, 各段階での膜電位について, 任意の0.79秒(約2周期分)のデータを用いて比較を行った. ここでは代表的にL型CaチャネルとT型Caチャネルの結果についてのせる
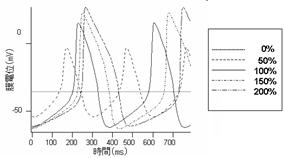
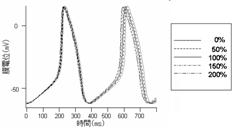
図2左図がL型Caチャネル、右図がT型Caチャネルの活性の変化と膜電位の様子を示したもの
2.2.
Krチャネル抑制の影響
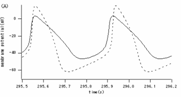
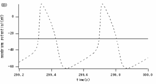
Krチャネルコンダクタンスを100%から0%まで5%刻みでダウンレギュレートすると, 55%では自律的な活動電位が保たれるが, 50%では, 活動電位が停止するという分岐現象がみられた. (Figure1)
|
図3 Krチャネルの活性変化による膜電位への影響 各グラフについて, 点線が正常状態(Krコンダクタンス100%)の膜電位を表す. 実線がダウンレギュレート後の膜電位である. (A) Krコンダクタンス=55%(縦軸:膜電位(mV) 横軸:時間(ms)) (B) Krコンダクタンス=50%(縦軸:膜電位(mV) 横軸:時間(ms)) |
生体実験の定量的なデータを用いて, モデルの分岐現象を検証した. モデルは分岐を再現しただけはなく, Krチャネルブロックの効果として生体実験で示されている, 活動電位延長効果も再現した.(table1)

表2 0. 1μmol/L E-4031投与時の活動電位パラメータとモデルの比較
A: 自律的な活動電位を示す洞房結節細胞(n=5); B: 0. 1 µmol/L E-4031の投与後, 自律的な活動電位が消失した心筋細胞(n=5) (A,B[3])C:in silicoにおける, gKr=53. 07%の洞房結節細胞D: in silicoにおける, gKr=53. 06%の洞房結節細胞
DDR:拡張期脱分極速度MDP:最大拡張期電位,APA:活動電位振幅,APD100:100%再分極での, 活動電位持続時間