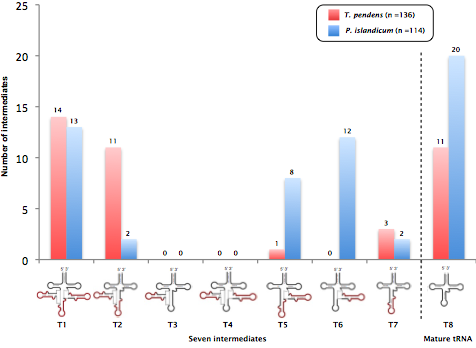
図1. 塩基配列決定により得られたプロセシング中間体一覧
タンパク質は生命活動の維持に不可欠な物質であり,Transfer RNA (tRNA)はタンパク質合成に関与する重要分子である.我々SPLITSプロジェクトでは,これまでtRNA遺伝子予測ソフトウエアの開発,および,それを用いた新規tRNA探索やデータベース開発を行うなど,超好熱性好酸性古細菌を中心とした複数の生物種において, イントロンを最大3つ介在する新規tRNAの存在を明らかにしてきた.しかし,これらのtRNAが実際に生体内に存在するのかや,そのスプライシング機構は詳しく理解されていない.そこで我々は3つのイントロンを介在すると予測されたThermofilum pendensなどを対象に,in vivoを中心としたスプライシング系を構築してプロセシング中間体を調査した.その結果,生体内において3つのイントロンを介在型するpre-tRNAの存在を確認することに成功し,さらに,イントロンが切除される順番には厳密な決まりがあり段階的スプライシングが行われている可能性を示唆することも出来た.また,それらの順番にはイントロン-エクソン間で形成されるスプライシングモチーフであるBulge-Helix-Bulge構造の自由エネルギーが深く関与していることが明らかとなったので以下に報告する.
地球上に生息するといわれている生物の細胞は主にタンパク質によって構成されており,タンパク質は細菌や植物やヒトなどの全ての生物において生命活動を維持するための重要物質である.そのため,生命を理解する上でタンパク質合成に関与するtRNAなどは非常に貴重な研究対象であると言われている.我々SPLITSプロジェクトでは,これまでtRNA遺伝子予測ソフトウエアの開発,および,それを用いた新規tRNA探索などの研究を続けてきた(Sugahara et al. 2006;Sugahara et al. 2007;sugahara et al. 2008).
古細菌tRNAのスプライシングは,古細菌間で普遍的に知られているBulge-Helix-Bulge (BHB) モチーフという特徴的な構造をエンドヌクレアーゼが認識し,イントロンが切断されるという決まりに従い進行する.BHBモチーフとは,前駆体RNAにおいてエクソンとイントロンの境界で形成されるもので,通常20〜200塩基程度で構成されており,主な形として4塩基のヘリックス構造の両脇を3塩基のバルジ構造が挟むhBHBh’構造,バルジ構造の一方が欠損しているHBh’構造,ループ部分にエクソンが含まれるHBL構造がある(Marck and Grosjean 2003).また,イントロンを切断する役割を担うのがエンドヌクレアーゼで,これは核酸配列の内部から核酸を切除する酵素であり,古細菌のスプライシングエンドヌクレアーゼはEndA遺伝子から発現するタンパク質複合体より形成されている.
しかし,これまで先攻研究に用いられてきたtRNAはイントロンを1つ特定の場所に介在するものに限定されており,複数イントロンを介在するtRNAを用いた例はあまり報告されていない (Tocchini et al. 2005a : Tocchini et al. 2005b : Song and Markley 2007).そのため,我々が予測したイントロンを3つ介在するtRNAの実験的な検証は行われておらず,詳しいスプライシングのメカニズムなどは解明されていない.そこで,本研究では情報学的手法により予測された結果をin vivoを中心としたスプライシング系を構築することにより検証した.古細菌という進化系統樹において比較的古い,生命の起源に近い枝から派生したとされている生物において,全生物において普遍的なタンパク質合成に深く関与するtRNA遺伝子を研究することは,生命の理解や進化を類推する上で非常に重要な論点になると思われる.
tRNA予測ソフトウエアであるSPLITSを中心に,情報学的手法より予測された新規tRNA中からイントロンを3つ介在すると予測されたThermofilum penden (T. pendens) とPyrobaculum islandicum (P. islandicum) を対象とし,それぞれの菌体をドイツDSMZ社より購入した.それぞれからTotal RNAを調製し,特異的なプライマーを用いてRT-PCRにより複数のプロセシング中間体を増幅させ,その後それらの断片の塩基配列を決定することでプロセシングの動態を塩基配列レベルで明らかにした.
今回はT. pendensとP. islandicumの両者において塩基配列決定を200ずつ決定した.しかし,プライマー部分のみ検出されたものや,他のtRNA配列,エラーなどを引くと,有用な塩基配列数はT. pendensで136,P. islandicumで114であった.さらに,情報学的に予測できる3つのイントロンを介在するtRNAのプロセシング中間体は成熟型tRNAとそれ以外で7つ存在するが,今回得られたこれら目的のプロセシング中間体数はT. pendensで29,P. islandicumで37となった.それをまとめた結果が図1である.

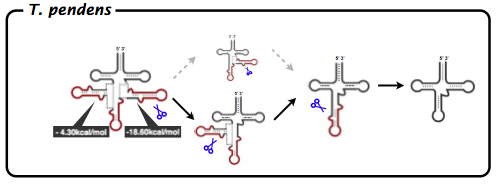
T. pendensにおいて検出された5つの中間体から考え得るプロセシング進行模式図を図2に示す.T. pendensにおけるプロセシングは,殆どの場合まず3’側のイントロンが切断され,その後5’側のイントロンが切断される.そして,両者のイントロンが切り取られてからアンチコドン部分でBHBモチーフが形成されイントロンが切断される.また,このスプライシングの順序には,それぞれのイントロンとエクソン間で形成されるBHBモチーフの自由エネルギーと深い関係があることも判明した.我々のこれまでの研究により,情報学的にもアンチコドン部分のイントロンは両者のイントロンが切り取られることで,初めてBHBモチーフが形成されると予測されてきた.また,tRNA遺伝子を予測した際に算出された3’側と5’側のBHBモチーフの自由エネルギーに注目した結果,両者で形成されるBHBモチーフの自由エネルギーには約4倍の差があることが分かった(Sugahara et al. 2007).3’側が-18.80kcal/mol で,5’側が-4.30mol/kal であったことから,自由エネルギー的に安定している3’側からエンドヌクレアーゼが認識し,イントロンが切り取られるのではないかと考えられる.
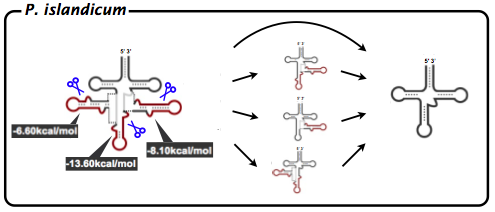
P. islandicumで検出された中間体から考え得るプロセシング進行模式図を図3に示す.P. islandicumで検出されたのは,3つのイントロンを介在するtRNA,3’側のイントロンが1つない中間体,5’側のイントロンが1つない中間体,5’側とアンチコドン部分のイントロンがない中間体,そして成熟型tRNAなど,T. pendensでは見られなかった中間体も含まれていた.これより,T. pendensのような厳密な段階的スプライシングは起こっていないと考えられる結果となった.また,P. islandicumにおいても,それぞれの自由エネルギーを比較してみたところ,3’側が-8.10kcal/mol,5’側が-6.60kcal/mol,アンチコドン部分が-13.60kcal/molであった.つまり,自由エネルギーに大差がないP. islandicumではどのイントロンからも切り取られることが可能で,無段階のスプライシングが行われていると考えられる.
我々はこれまで情報学的に新規tRNA予測を行ってきたが,それらが実際に生体内に存在するのか,存在する場合そのスプライシングのメカニズムは理解されていなかった.そこで,今回はイントロンを3つ介在すると予測されたtRNAを対象に,in vivoを中心としたプロセシング中間体を観察する実験を行ってきた.T. pendensとP. islandicumの2種の古細菌を対象に研究を進めたところ,両者で検出されるプロセシング中間体には違いがあり,一方はスプライシングに厳密な順番が存在するのに対し,もう一方では順番のない無段階スプライシングの可能性を示す結果を得ることができた.さらに,スプライシングの順にはイントロンとエクソン間で形成されるBHBモチーフの自由エネルギーが深く関与していることも分かり,これらは事前に行ってきた予備実験とも一致する結果となった.また,通常のスプライシングの決まりに従うと発生しない中間体も数多く検出され,これらが一体何を意味するのか今後検証していきたい.本研究の結果はtRNAの構造が生体内においてダイナミックに変化していることを指示する大変興味深いものとなった.今後さらに研究を続け,生命の起源や進化についても議論をしていきたい.
Marck, C. and Grosjean, H. 2003. Identification of BHB splicing motifs in intron-containing tRNAs from 18 archaea: evolutionary implications. RNA. 9 : 1516–1531.
Sugahara, J., Yachie, N., Sekine, Y., Soma, A., Matsui, M., Tomita, M., and Kanai, A. 2006. SPLITS: a new program for predicting split and intron-containing tRNA genes at the genome level. In Silico Biology. 6 : 0039.
Sugahara, J., Yachie, N., Arakawa, K., Tomita, M. 2007. In silico screening of Archaeal tRNA encoding genes having bulge-helix-bulge splicing motifs. RNA. 13 : 671-682.
Sugahara, J., Kikuta, K., Fujishima, K., Yachie, N., Tomita, M. and Kanai, A. 2008. Comprehensive analysis of archaeal tRNA genes reveals rapid increase of tRNA introns in the order Thermoproteales. Mol Biol Evol. 25 : 2709-2716.
Tocchini-Valentini, GD., Fruscoloni, P., Tocchini-Valentini, GP. 2005a. Coevolution of tRNA intron motifs and tRNA endonuclease architecture in Archaea. Proc Natl Acad Sci U.S.A. 102 : 15418-15422.
Tocchini-Valentini, GD., Fruscoloni, P., Tocchini-Valentini, GP. 2005b. S Structure, function, and evolution of the tRNA endonucleases of Archaea: an example of subfunctionalization. Proc Natl Acad Sci U.S.A. 102 : 8933-8.
Tocchini-Valentini, GD., Fruscoloni, P., Tocchini-Valentini, GP. 2007. The dawn of dominance by the mature domain in tRNA splicing. Proc Natl Acad Sci U S A. 104 : 12300-5.